Elektrolys: En Djupgående Förklaring av en Fascinerande Process
Vad är Elektrolys?
Elektrolys är en kemisk process där elektrisk ström används för att driva en icke-spontan kemisk reaktion. I grund och botten handlar det om att bryta ner kemiska föreningar genom att tillföra elektrisk energi. Denna process är central inom många industriella tillämpningar och forskningsområden.

För att elektrolys ska kunna ske behövs en elektrolyt, som är en substans som innehåller fria joner och kan leda elektricitet. Detta kan vara en smälta av ett salt, en lösning av ett salt i vatten eller en annan lämplig vätska. Elektroder, som är ledande material, sänks ner i elektrolyten. En strömkälla kopplas till elektroderna, vilket skapar en elektrisk potential mellan dem.
Grundläggande Principer
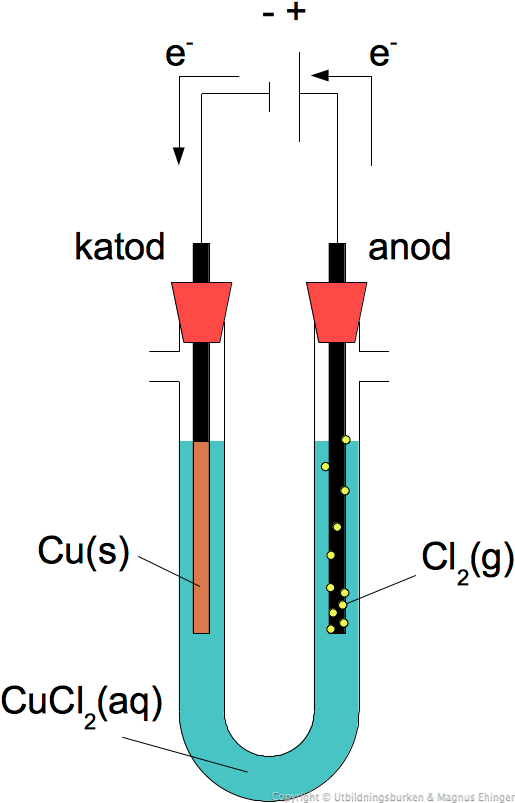
Under elektrolys sker oxidation vid anoden (den positiva elektroden) och reduktion vid katoden (den negativa elektroden). Jonerna i elektrolyten rör sig mot elektroderna med motsatt laddning. Positiva joner (katjoner) rör sig mot katoden, där de tar upp elektroner och reduceras. Negativa joner (anjoner) rör sig mot anoden, där de avger elektroner och oxideras.
Denna process kan beskrivas med hjälp av Faradays lagar om elektrolys, som kvantifierar mängden ämnen som omvandlas vid elektroderna i förhållande till den elektriska laddningen som passerar genom systemet.
Användningsområden för Elektrolys

Elektrolys har en mängd olika tillämpningar inom olika industrier och forskningsområden. Här är några av de mest betydelsefulla:
-

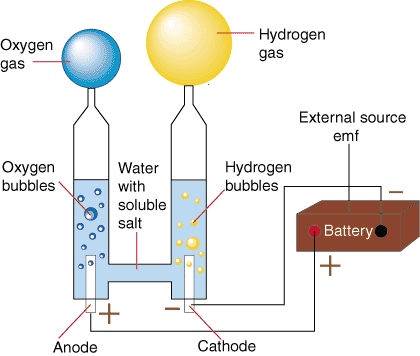
Vattenelektrolys: Detta är en process där vatten bryts ner till vätgas och syrgas med hjälp av elektrisk ström. Vätgasen kan sedan användas som ett rent bränsle.
-
Metallurgi: Elektrolys används för att extrahera och rena metaller från deras malmer. Till exempel används elektrolys för att producera aluminium från bauxit.
-
Galvanisering: Detta är en process där ett tunt lager av en metall avsätts på en annan metall med hjälp av elektrolys. Galvanisering används för att skydda metaller mot korrosion och för att förbättra deras utseende.
-
Batterier: Elektrolys är en central process i laddningsbara batterier, där elektrisk energi omvandlas till kemisk energi och vice versa.
-
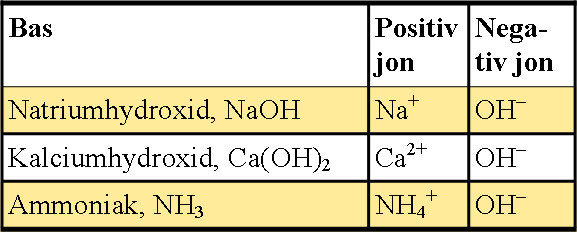
Kemisk industri: Elektrolys används för att producera en mängd olika kemikalier, inklusive klor, natriumhydroxid och väteperoxid.
Elektrolysens Roll i Hållbarhet
Elektrolys spelar en viktig roll i övergången till en mer hållbar framtid. Vattenelektrolys, som nämnts tidigare, kan användas för att producera vätgas, ett rent bränsle som kan ersätta fossila bränslen. Dessutom kan elektrolys användas för att rena avloppsvatten och återvinna värdefulla ämnen från industriella avfall.
Forskning pågår för att utveckla mer effektiva och kostnadseffektiva elektrolysmetoder, vilket kan bidra till att göra hållbara tekniker mer tillgängliga.
Framtida Potential
Elektrolys har en enorm potential att revolutionera många industrier och bidra till att lösa några av våra största utmaningar, inklusive klimatförändringar och energiförsörjning. Med fortsatta framsteg inom materialvetenskap och elektrokemi kan vi förvänta oss att se ännu fler innovativa tillämpningar av elektrolys i framtiden.

Den snabba utvecklingen av förnybar energi, som sol- och vindkraft, skapar nya möjligheter att använda elektrolys för att lagra överskottsenergi i form av vätgas. Detta kan bidra till att skapa ett mer flexibelt och hållbart energisystem.
Copyright © [Ditt Namn/Företag] 2023. Alla rättigheter reserverade.