Elektrolyscell: En Djupgående Förklaring
Vad är en Elektrolyscell?
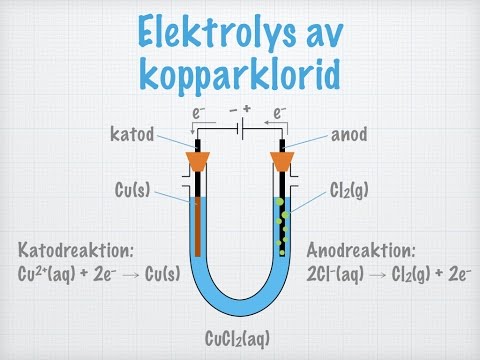
En elektrolyscell är en anordning som använder elektrisk energi för att driva en icke-spontan kemisk reaktion, en process som kallas elektrolys. I grund och botten omvandlar den elektrisk energi till kemisk energi. Denna process är fundamental inom många industriella och vetenskapliga områden.
Den består av två elektroder, en anod och en katod, nedsänkta i en elektrolyt. Elektrolyten är en lösning eller en smälta som innehåller joner som kan röra sig fritt.
Hur Fungerar en Elektrolyscell?

När en elektrisk ström appliceras på elektroderna, tvingas jonerna i elektrolyten att röra sig. Negativa joner (anjoner) rör sig mot den positiva anoden, där de oxideras (förlorar elektroner). Positiva joner (katjoner) rör sig mot den negativa katoden, där de reduceras (tar upp elektroner). Denna process leder till kemiska förändringar vid elektroderna.

Den elektriska strömmen driver reaktionen, vilket gör att ämnen kan separeras eller bildas som annars inte skulle kunna skapas spontant.
Viktiga Komponenter i en Elektrolyscell
- Anod: Den positiva elektroden där oxidation sker.
- Katod: Den negativa elektroden där reduktion sker.
- Elektrolyt: En lösning eller smälta som innehåller joner.
- Strömkälla: Levererar den elektriska strömmen.

Tillämpningar av Elektrolysceller

Elektrolysceller används i en mängd olika tillämpningar, inklusive:
- Elektroplätering: Att belägga ett metallföremål med ett tunt lager av en annan metall.
- Framställning av kemikalier: Som klor, natriumhydroxid och aluminium.
- Vattenelektrolys: Att dela upp vatten i vätgas och syrgas.
- Batteriladdning: Att återställa kemiska reaktioner i uppladdningsbara batterier.
- Raffinering av metaller: Att rena metaller genom elektrolys.

Speciellt vattenelektrolys är av stor betydelse i arbetet mot en mer hållbar framtid.
Elektrolysceller i Framtiden
Forskning och utveckling inom elektrolyscellteknik fortsätter att driva fram innovationer. Effektivare och mer hållbara elektrolysceller är avgörande för att uppnå en grönare industri och energisektor. Med framsteg inom materialvetenskap och elektrokemi kan vi förvänta oss att se ännu fler tillämpningar av denna teknik i framtiden.
Den fortsatta utvecklingen av effektiva elektrolysceller för vätgasproduktion är avgörande för att skapa en hållbar energiframtid.
Vanliga Frågor om Elektrolysceller
- Vad är skillnaden mellan en elektrolyscell och ett galvaniskt element?
En elektrolyscell använder elektrisk energi för att driva en icke-spontan reaktion, medan ett galvaniskt element omvandlar kemisk energi till elektrisk energi genom en spontan reaktion.
- Vilka faktorer påverkar effektiviteten hos en elektrolyscell?
Faktorer som elektrodmaterial, elektrolytsammansättning, temperatur och strömtäthet påverkar effektiviteten.
- Är elektrolysceller miljövänliga?
Beroende på strömkällan kan elektrolysceller vara miljövänliga, särskilt när de drivs av förnybar energi.